Introdução - Objetivo
A detecção do HPV é uma prioridade global de saúde. O HPV de alto risco (HR-HPV) é uma das principais causas de câncer cervical, enquanto o HPV de baixo risco (LR-HPV) está associado a lesões benignas, como verrugas genitais. Testes confiáveis para HPV exigem desempenho laboratorial padronizado, e os Programas Externos de Avaliação da Qualidade (PEQA) desempenham um papel vital para garantir a precisão e a harmonização. Este estudo comparou o desempenho laboratorial em um PEQA para detecção molecular de HR-HPV e LR-HPV por PCR/qPCR, organizado por um provedor credenciado pela ABNT NBR ISO/IEC 17043:2011.
Métodos
Amostras líquidas de escovado cervical ou lisado celular foram utilizadas no PEQA. Entre 2020 e 2024, os laboratórios receberam duas amostras trimestrais para avaliar a acurácia (AC), a sensibilidade (SE) e a especificidade (SP). Essas métricas de desempenho foram avaliadas e comparadas entre PCR/qPCR para HPV de alto e baixo risco usando testes qui-quadrado e odds ratio. As tendências de AC para HR-HPV e LR-HPV ao longo do tempo foram analisadas usando o teste de Mann-Kendall.
Resultados
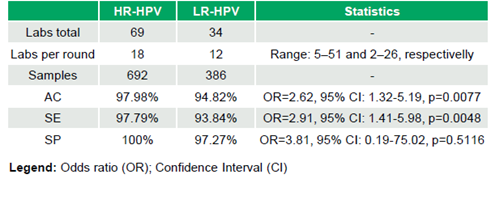
69 laboratórios (mediana de 18 laboratórios/rodada, intervalo de 5 a 51; 692 conjuntos de dados) participaram da avaliação de HR-HPV e 34 laboratórios (mediana de 12 laboratórios/rodada, intervalo de 2 a 26; 386 conjuntos de dados) na avaliação de LR-HPV. Os resultados do HR-HPV foram 97,98% (678/692) AC, 97,79% (620/634) SE e 100% (58/58) ES, enquanto o LR-HPV atingiu 94,82% (366/386) AC, 93,84% (259/276) SE e 97,27% (107/110) ES. Diferenças significativas na SE (OR=2,91, IC95%: 1,41–5,98, p=0,0048) e AC (OR=2,62, IC95%: 1,32–5,19, p=0,0077) favoreceram o HR-HPV, enquanto a ES foi comparável (OR=3,81, IC95%: 0,19–75,02, p=0,5116) (Tabela 1). Não foram observadas tendências significativas na AC ao longo do tempo para os testes de HPV de alto risco (τ = -0,046, p = 0,795) ou de baixo risco (τ = 0,3, p = 0,098).
Conclusões
Ambas as avaliações demonstraram forte desempenho, com o HR-HPV apresentando melhor sensibilidade e acurácia, enquanto a especificidade foi semelhante. Não foram observadas tendências significativas na acurácia ao longo do tempo, indicando estabilidade sem alterações ao longo do tempo. A detecção do LR-HPV continua sendo crucial para o manejo de lesões, permitindo um tratamento com boa relação custo-benefício, reduzindo a transmissão e apoiando estratégias de saúde pública. Este estudo destaca que os ensaios de PCR/qPCR para LR-HPV têm espaço para melhorias para atender aos padrões de HR-HPV, enfatizando a necessidade de refinamento contínuo e avaliações de qualidade.
Referências
WHO guideline for screening and treatment of cervical pre-cancer lesions for cervical cancer prevention, second edition:Use of mRNA tests for human papillomavirus (HPV)-World Health Organization 2021.
Human papillomavirus (HPV) nucleic acid amplification tests (NAATs) to screen for cervical pre-cancer lesions and prevent cervical cancer: policy brief-World Health Organization 2022.
Okada PA, Mitrat S, Rojanawiwat A. External quality assessment program for human papillomaviruses DNA testing in Thailand. Pract Lab Med. 2023 Dec 26; 38: e00352. doi: 10.1016/j.plabm. 2023. e00352. PMID: 38292923; PMCID: PMC10825476.